Giải bài 42 hoá học 9: luyện tập chương 4
Lớp 2 - kết nối tri thức
Lớp 2 - Cánh diều
Lớp 2 - Chân trời sáng tạo
Tài liệu tham khảo
Lớp 3Sách giáo khoa
Tài liệu tham khảo
Sách VNEN
Lớp 4Sách giáo khoa
Sách/Vở bài xích tập
Đề thi
Lớp 5Sách giáo khoa
Sách/Vở bài bác tập
Đề thi
Lớp 6Lớp 6 - kết nối tri thức
Lớp 6 - Cánh diều
Lớp 6 - Chân trời sáng tạo
Sách/Vở bài xích tập
Đề thi
Chuyên đề & Trắc nghiệm
Lớp 7Sách giáo khoa
Sách/Vở bài tập
Đề thi
Chuyên đề & Trắc nghiệm
Lớp 8Sách giáo khoa
Sách/Vở bài xích tập
Đề thi
Chuyên đề & Trắc nghiệm
Lớp 9Sách giáo khoa
Sách/Vở bài xích tập
Đề thi
Chuyên đề và Trắc nghiệm
Lớp 10Sách giáo khoa
Sách/Vở bài bác tập
Đề thi
Chuyên đề & Trắc nghiệm
Lớp 11Sách giáo khoa
Sách/Vở bài bác tập
Đề thi
Chuyên đề và Trắc nghiệm
Lớp 12Sách giáo khoa
Sách/Vở bài xích tập
Đề thi
Chuyên đề và Trắc nghiệm
ITNgữ pháp giờ đồng hồ Anh
Lập trình Java
Phát triển web
Lập trình C, C++, Python
Cơ sở dữ liệu

Các dạng bài tập chất hóa học lớp 9Chương 1: các loại hợp chất vô cơChương 2: Kim loạiChương 3: Phi kim. Qua quýt về bảng tuần hoàn các nguyên tố hóa họcChương 4: Hiđrocacbon. Nhiên liệuChương 5: Dẫn xuất của Hiđrocacbon. Polime
Để học xuất sắc Hóa học tập lớp 9, phần dưới tổng hợp lý thuyết và bài tập trắc nghiệm (có đáp án) chất hóa học lớp 9 Chương 4: Hiđrocacbon. Nhiên liệu. Chúng ta vào tên dạng hoặc Xem cụ thể để xem những chuyên đề hóa học 9 tương ứng.
Bạn đang xem: Giải bài 42 hoá học 9: luyện tập chương 4
Mục lục Hóa 9 Chương 4: Hiđrocacbon. Nhiên liệu
I. Triết lý & Trắc nghiệm theo bài xích học
II. Những dạng bài bác tập
Cách viết Công thức kết cấu của những hợp hóa học hữu cơ
Lý thuyết và phương pháp giải
Lý thuyết yêu cầu nhớ
- các hợp hóa học hữu cơ bao gồm cùng phương pháp phân tử dẫu vậy có cấu trúc hóa học khác nhau, dẫn tới tính chất hóa học khác biệt được điện thoại tư vấn là những chất đồng phân của nhau.
- Ankan là mọi hidrocacbon no mạch hở tất cả công thức thông thường CnH2n+2 (n ≥ 1).
- Xicloankan là hidrocacbon không no, mạch hở cất 1 nối song C=C vào phân tử, tất cả công thức chung là CnH2n (n ≥ 2).
- Ankadien: là hidrocacbon mạch hở, cất 2 nối đôi trong phân tử, gồm công thức phổ biến là CnH2n-2 (n ≥ 3).
- Ankin là hidrocacbon mạch hở, đựng một nối tía C ≡ C trong phân tử, gồm công thức bình thường CnH2n-2 (n ≥ 3).
- Hidrocacbon thơm (aren) là loại hidrocacbon trong công thức phân tử bao gồm một hay những nhân bezen, đại diện thay mặt cho dãy đồng đẳng aren là phân tử benzen có công thức bao quát CnH2n-6 (n ≥ 6).
Phương pháp chung:
Bước 1: Tính độ bất bão hòa (số links và vòng).
Bước 2: Viết cấu tạo mạch cacbon (không phân nhánh, bao gồm nhánh, vòng) cùng đưa liên kết bội (đôi, ba) vào mạch cacbon giả dụ có.
Bước 3: Đưa team chức vào mạch cacbon (thông thường những nhóm chức chứa cacbon thường xuyên được đưa luôn vào mạch ở bước 3). để ý đến trường đúng theo kém bền hoặc ko tồn tại của tập thể nhóm chức (ví dụ nhóm –OH ko bền và sẽ bị chuyển vị khi gắn với cacbon có links bội).
Xem thêm: Results For : Hiep Dam Chi Dau, 'Hiep Dam Chi Dau' Search
Bước 4: Điền số H vào để đảm bảo đủ hóa trị của những nguyên tố, tiếp đến xét đồng phân hình học ví như có. Chú ý với những bài tập trắc nghiệm rất có thể không bắt buộc điền số nguyên tử H.
♦ khẳng định độ bất bão hõa của hợp chất hữu cơ CxHyOzNtXv theo công thức:
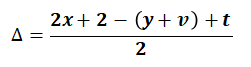
Chú ý:
-Công thức tính sinh sống trên chỉ vận dụng cho hợp chất cộng hóa trị.
-Các yếu tố hóa trị II như oxi, diêm sinh không tác động tới độ bất bão hòa.
Bài tập vận dụng
Bài 1: Hợp hóa học C5H10 gồm bao nhiêu đồng phân cấu tạo của anken?
Hướng dẫn:
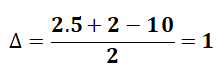
Vì C5H10 là anken yêu cầu C5H10 là mạch hở, có 1 liên kết pi.
Có 5 đồng phân anken của C5H10
CH3-CH2-CH2-CH=CH2
CH3-CH2-CH=CH-CH3
CH3-CH2-C(CH3)=CH2
CH3-CH=C(CH3)-CH3
CH3-CH(CH3)-CH=CH2
Bài 2: gồm bao nhiêu đồng phân cấu tạo có cách làm phân tử C6H14?
Hướng dẫn:
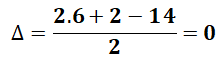
⇒ Ankan ⇒ Chỉ có liên kết đơn
Vậy C6H14 chỉ gồm 5 đồng phân cấu tạo.
CH3-CH2-CH2-CH2-CH2-CH3
CH3-CH(CH3)-CH2-CH2-CH3
CH3-CH2-CH(CH3)-CH2-CH3
CH3-CH(CH3)-CH(CH3)-CH3
CH3-C(CH3)2-CH2-CH3
Cách lập bí quyết phân tử hợp chất hữu cơ
Lý thuyết và phương pháp giải
Để giải dạng bài bác này, thứ nhất ta cần xác định hợp hóa học hữu cơ nên tìm bao hàm nguyên tố gì, tiếp đến tùy theo đề bài để giải bài bác toán.
Giả thiết bài xích toán:
Đốt cháy a (gam) hợp chất hữu cơ A thu được m (g) CO2, m (g) H2O cùng m (g) N2 (nếu có). Tính M trọng lượng mol của A (mA) yêu mong lập phương pháp phân tử của A.
Các cách lập cách làm phân tử:
Bước 1: Định lượng những nguyên tố trong A.
- search C: nhờ vào CO2
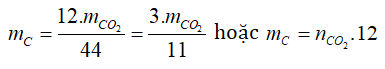
- tìm kiếm H: phụ thuộc H2O.
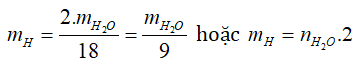
- tra cứu N: nhờ vào N2.
mN = mN2 hoặc mN = nN2.28
- tìm O: Dùng cách thức loại suy.
mO = a - (mC + mH + mN)
Bước 2: Tính trọng lượng phân tử giao động của hợp hóa học hữu cơ.
- phụ thuộc vào tỉ khối hơi:
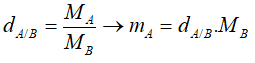
Nếu B là không gian thì MB = 29.
- nhờ vào số mol cùng khối lượng:
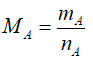
Bước 3: Lập phương pháp phân tử của A.
- Ở cách này, ta gồm 3 cách để lập bí quyết phân tử của A.
● giải pháp 1: dựa vào thành phần cân nặng của những nguyên tố trong phân tử hợp hóa học hữu cơ. Đối với phương pháp này hay phổ biến so với bài toán cơ phiên bản cho trước MA.
Ta bao gồm công thức tổng thể CxHyOzNt.
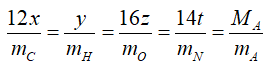
Hoặc nếu việc cho phần trăm khối lượng của các %C ta có công thức:
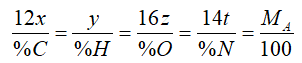
Thay các giá trị sẽ biết vào công tác thức trên suy ra các giá trị x, y, z, t, kế tiếp thay vào CTTQ ta được cách làm phân tử yêu cầu lập.
● bí quyết 2: Lập bí quyết phân tử qua phương pháp thực nghiệm. Đối với cách này thường dùng làm giải những bài toán nhưng mà yêu ước lập bí quyết nguyên hay việc cho thiếu mang thiết để tính MA.
Trước tiên ta lập tỷ lệ số nguyên tử giữa các nguyên tố
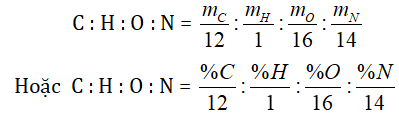
= a : b : c : d (là tỉ trọng số nguyên, về tối giản)
Suy ra công thức thực nghiệm (CaHbOcNd)n.
Trong kia n ≥ 1 (là số nguyên): gọi là thông số thực nghiệm.
Dựa vào MA hoặc trả thiết của đề đến suy ra n, cầm vào bí quyết thực nghiệm suy ra công thức phân tử phải lập.
● biện pháp 3: nhờ vào phương trình cháy.
Giáo viên chỉ dẫn cho học viên phương trình cháy tổng quát nhất và cách điền số vào phương trình.
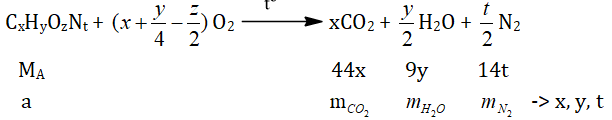
Sau đó dựa vào MA = 12x + y + 16z + 14t → Z
Bài tập vận dụng
Bài 1: Phân tử hợp hóa học hữu cơ A bao gồm 2 nguyên tố. Đốt cháy trọn vẹn 3 gam hóa học A nhận được 5,4 gam nước. Hãy khẳng định công thức phân tử của A. Biết khối lượng mol của A là 30 gam.
Hướng dẫn:
Cách 1
Hợp chất hữu gồm A bao gồm 2 nguyên tố, khi đốt cháy thu được nước
→ A chứa 2 nhân tố C với H
nH2O = 5,4/18 = 0,3 mol
→ nH = 2. 0,3 = 0,6 mol → mH = 0,6 gam
→ mC = 3 - 0,6 = 2,4 gam → nC = 2,4/12= 0,2 mol
→ nC : nH = 0,2 : 0,6 = 1 : 3
→ Công thức đơn giản dễ dàng nhất của A là (CH3)n
Mà MA = 30 → 15n = 30 → n = 2
→ CTPT của A là C2H6
Cách 2
A là chất hữu cơ đề xuất trong A đề nghị chứa yếu tắc C.
Khi đốt cháy A thu được nước → trong A phải tất cả H
Mặt khác A chứa 2 nguyên tố cần A có công thức CxHy
nA = 3/30 = 0,1 ml; nH2O = 5,4/18 = 0,3 mol
4 CxHy + O2 → 4x CO2 + 2y H2O
4.…………………………………2y
0,1………………………………0,3
→ 0,1.2y = 4.0,3 → y = 6
Mặt khác 12x+y = 30 → 12x + 6 = 30 → x = 2
→ CTPT của A là: C2H6
Bài 2: Đốt cháy 3 gam một chất hữu cơ A chiếm được 6,6 gam CO2 với 3,6 gam H2O. Khẳng định công thức phân tử của A, biết cân nặng mol phân tử của A là 60 gam
Hướng dẫn:
nCO2 = 6,6/44=0,15 mol; nH2O = 3,6/18 = 0,2 mol
→ nC = 0,15 mol; nH = 0,2.2 = 0,4 mol→ mC = 12.0,15 = 1,8 gam; mH = 0,4.1 = 0,4 gam
→ mC + mH = 1,8 + 0,4 = 2,2 gam A
→ vào A còn có O (vì khi đốt cháy chỉ chiếm được CO2 với H2O)
→ mO = 3 – (mC + mH) = 3 – 2,2 = 0,8 mol → nO = 0,8/16 = 0,05 mol
→ nC : nH : nO = 0,15 : 0,4 : 0,05 = 3 : 8 :1
→ Công thức đơn giản nhất của A là (C3H8O)n
MA = 60 → 60n = 60 → n = 1
→ CTPT của A là C3H8O
Cách giải bài toán đốt cháy hidrocacbon
Lý thuyết và phương thức giải
Hidrocacbon CxHy hoặc CnH2n+2-2k (n ≥ 1,

 Trương gia bình ly hôn
Trương gia bình ly hôn Giá giẻ hay giá rẻ
Giá giẻ hay giá rẻ Bảng phrasal verb đầy đủ
Bảng phrasal verb đầy đủ Luffy ăn trái ác quỷ thứ 2
Luffy ăn trái ác quỷ thứ 2 Giá thuốc h5000 của pháp
Giá thuốc h5000 của pháp Mã quà tặng ch play
Mã quà tặng ch play Nhà tuyết ở quận 7
Nhà tuyết ở quận 7 Quy tắc cái đinh ốc
Quy tắc cái đinh ốc Mẫu chữ song hỷ đẹp
Mẫu chữ song hỷ đẹp Các bộ phận của bàn chân
Các bộ phận của bàn chân Trai bao 1
Trai bao 1 Chọn vải may quần ống suông
Chọn vải may quần ống suông Gắp n giá bao nhiêu
Gắp n giá bao nhiêu Như ý phương phi vn2
Như ý phương phi vn2 Sữa rửa mặt hatomugi thật giả
Sữa rửa mặt hatomugi thật giả